中美欧加快通道对比分析
欢迎关注微信公众号:注册圈,阅读更多精彩文章(微信号:XJ50080)
药物研发流程和里程碑事件
▲药物研发周期
 [backcolor=rgba(18, 18, 18, 0.5)]​ [backcolor=rgba(18, 18, 18, 0.5)]​
编辑切换为居中
添加图片注释,不超过 140 字(可选)
- Milestone 1 –Submitting an IND application(里程碑1 -提交IND申请)
- Milestone 2 –Initiating the Phase I trial(里程碑2 -启动1期临床试验)
- Milestone 3 –Conducting the pivotal Phase III trials(里程碑3 -进行关键的3期临床试验)
- Milestone 4 –Submission of the NDA/BLA(里程碑4 -提交NDA/BLA)
- Milestone 5 –Approval of the NDA/BLA(里程碑5 -批准NDA/BLA)
2020年版药品注册管理办法 第二章基本制度和要求
第十三条 国家药品监督管理局建立药品加快上市注册制度,支持以临床价值为导向的药物创新。对符合条件的药品注册申请,申请人可以申请适用突破性治疗药物、附条件批准、优先审评审批及特别审批程序。在药品研制和注册过程中,药品监督管理部门及其专业技术机构给予必要的技术指导、沟通交流、优先配置资源、缩短审评时限等政策和技术支持。
解读:利好的新政策,值得期待配套政策及技术要求。
威胁时事件发生后统一指挥、早期介入、快速高效、科学审批
中国药品加快上市注册程序
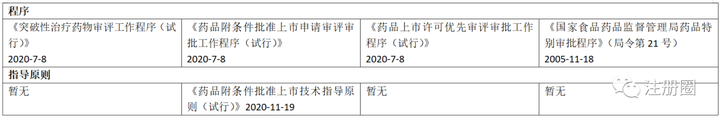
▲4个加快注册程序的当前法规
 [backcolor=rgba(18, 18, 18, 0.5)]​ [backcolor=rgba(18, 18, 18, 0.5)]​
编辑切换为居中
添加图片注释,不超过 140 字(可选)
 [backcolor=rgba(18, 18, 18, 0.5)]​ [backcolor=rgba(18, 18, 18, 0.5)]​
编辑切换为居中
添加图片注释,不超过 140 字(可选)
 [backcolor=rgba(18, 18, 18, 0.5)]​ [backcolor=rgba(18, 18, 18, 0.5)]​
编辑切换为居中
添加图片注释,不超过 140 字(可选)
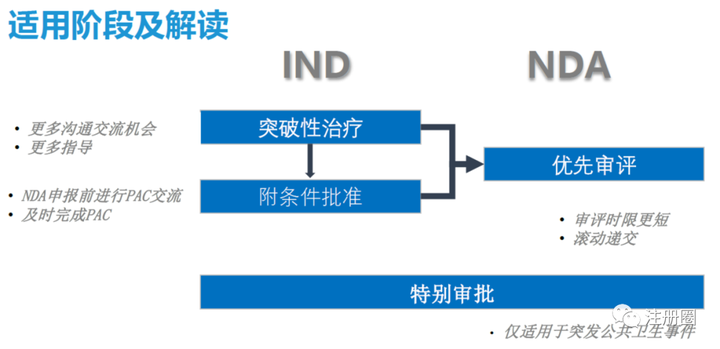
中美欧药品加快上市注册程序对比
 [backcolor=rgba(18, 18, 18, 0.5)]​ [backcolor=rgba(18, 18, 18, 0.5)]​
编辑切换为居中
添加图片注释,不超过 140 字(可选)
中美欧突破性治疗相关程序对比
▲中美欧突破性治疗相关程序对比
 [backcolor=rgba(18, 18, 18, 0.5)]​ [backcolor=rgba(18, 18, 18, 0.5)]​
编辑切换为居中
添加图片注释,不超过 140 字(可选)
 [backcolor=rgba(18, 18, 18, 0.5)]​ [backcolor=rgba(18, 18, 18, 0.5)]​
编辑切换为居中
添加图片注释,不超过 140 字(可选)
中美欧优先审评审批相关程序对比
▲中美欧优先审评审批相关程序对比
 [backcolor=rgba(18, 18, 18, 0.5)]​ [backcolor=rgba(18, 18, 18, 0.5)]​
编辑切换为居中
添加图片注释,不超过 140 字(可选)
 [backcolor=rgba(18, 18, 18, 0.5)]​ [backcolor=rgba(18, 18, 18, 0.5)]​
编辑切换为居中
添加图片注释,不超过 140 字(可选)
中美欧附条件批准相关程序对比
▲中美欧附条件批准相关程序对比
 [backcolor=rgba(18, 18, 18, 0.5)]​ [backcolor=rgba(18, 18, 18, 0.5)]​
编辑切换为居中
添加图片注释,不超过 140 字(可选)
 [backcolor=rgba(18, 18, 18, 0.5)]​ [backcolor=rgba(18, 18, 18, 0.5)]​
编辑切换为居中
添加图片注释,不超过 140 字(可选)
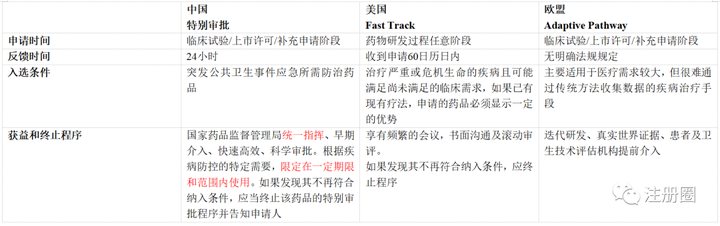
中美欧特别审批程序对比
▲中美欧特别审批程序对比
 [backcolor=rgba(18, 18, 18, 0.5)]​ [backcolor=rgba(18, 18, 18, 0.5)]​
编辑切换为居中
添加图片注释,不超过 140 字(可选)
药品加快上市注册-中国特色
 [backcolor=rgba(18, 18, 18, 0.5)]​ [backcolor=rgba(18, 18, 18, 0.5)]​
编辑切换为居中
添加图片注释,不超过 140 字(可选)
本文声明:本文搬运分享于公众号:[注册圈],仅供参考,小编对文中观点持中立态度,文中版权归原作者所有,文章篇幅有限,更多精彩请前往公众号查看。
|